5-Deazaflavine
NMR Spectroscopy - Hot Paper
5-Deazaflavine reagieren auch als Ein-Elektronenüberträger
Charakterisierung der elektronischen Struktur von 5-Deazaflavin-Radikalen durch photo-CIDNP-NMR
5-Deazaflavine sind Analoga der Flavinen. Dabei ist das N-5 Stickstoffatom im Isoalloxazin Ring durch ein Kohlenstoff-atom ersetzt.
Flavine sind weitverbreitete kovalent gebundene Cofaktoren in Enzymen, die reversibel ein oder zwei Elektronen aufnehmen oder abgeben können, und an einer Vielzahl an Redox-reaktionen in Organismen beteiligt sind. Zudem absorbieren sie auch im sichtbaren Wellenbereich. Die Photoreduktions-reaktionen unter Blaulicht werden z.B. von den Phototropinen für das lichtgerichtete Pflanzenwachstum, von Photolyasen, um die UV-Schaden an der DNA zu reparieren, und von Cryptochromen bei der Regulierung des Circadianen Rhythmus genutzt.
Die 5-Deazaflavine haben sich aufgrund der strukturellen Ähnlichkeit sehr wertvoll als Substituenten bei der Untersuchung der Reaktionsmechanismen in Flavoproteinen gezeigt. Dabei wurden sie bisher, anders als die Flavine, ausschließlich als Zwei-Elektronenüberträger postuliert, und deshalb eher zu den Nicotinamiden zugeordnet. Kürzlich konnte allerdings unter biologisch relevanten Reaktionsbedingungen die Radikalbildung (und damit der Ein-Elektronentransfer) von 5-Deazaflavinen indirekt beobachtet werden.
Wissenschaftlerinnen und Wissenschaftler am Institut für Physikalische Chemie der Universität Freiburg konnten jetzt erstmals die elektronische Struktur von 5-Deaza-FMN (5-Deaza-Flavinmononukleotid) bestimmen und so nachweisen, dass 5-Deazaflavine genauso wie die Flavine als Ein-Elektronenüberträger fungieren können.
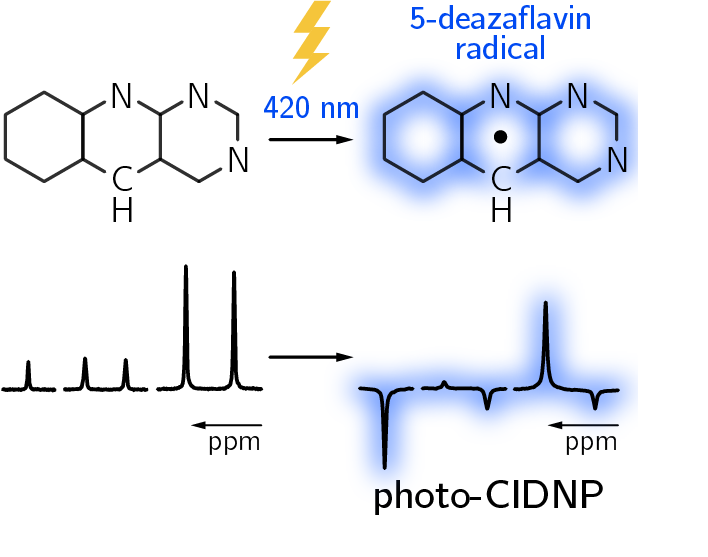
Die elektronische Charakterisierung erfolgte mittels photo-CIDNP (photo-chemically induced dynamic nuclear polarization, photochemisch induzierte dynamische Kernpolarisation), eine NMR-Methode, die besonders kurzlebige Radikale detektieren und untersuchen kann. Dazu wurde 5-Deaza-FMN mit L-Tryptophan als Modellsystem unter physiologischen Bedingungen in Lösung gebracht. Durch Anregung mit einem Laser wurde dann ein photoinduziertes Radikalpaar gebildet. Gekoppelt mit NMR-Spektroskopie lassen sich auf diese Weise hyperpolarisierte Kernspinzustände erzeugen. Die beobachteten Hyperpolarisationsmuster ermöglichen es, kurzlebige radikalische Zwischenstufen zu charakterisieren sowie die zugrundeliegenden Reaktionsmechanismen aufzudecken.
Der eindeutige Nachweis eines 5-Deaza-FMN-Radikals durch photo-CIDNP-Experimente erweitert das Reaktionsspektrum von 5-Deaza-FMN auf Ein-Elektrontransferreaktionen und wirft ein neues Licht auf die katalytische Rolle von 5-Deaza-Flavinen in biologischen Redoxprozessen.
Originalpublikation:
J. Wörner, S. Panter, B. Illarionov, A. Bacher, M. Fischer und S. Weber
Expanding Reaction Horizons: Evidence oft he 5-Deazaflavin radical through Photo-Chemically Induced Dynamic Nuclear Polarization
Angew. Chem. Int. Ed. 62 (2023), e202309334 (6 pages).
DOI: 10.1002/anie.202309334
Auch in deutscher Übersetzung:
J. Wörner, S. Panter, B. Illarionov, A. Bacher, M. Fischer und S. Weber
Erweiterung des Reaktionsspektrums: Nachweis des 5-Deazaflavin-Radikals durch photochemisch induzierte dynamische Kernpolarisation
Angewandte Chemie, 135 (2023), e202309334 (7 Seiten)
DOI:10.1002/ange.202309334
Kontakt:
Prof. Dr. Stefan Weber
Institut für Physikalische Chemie
Albert-Ludwigs-Universität Freiburg
Telefon: +49 761 / 203-6214
E-Mail: stefan.weber@physchem.uni-freiburg.de